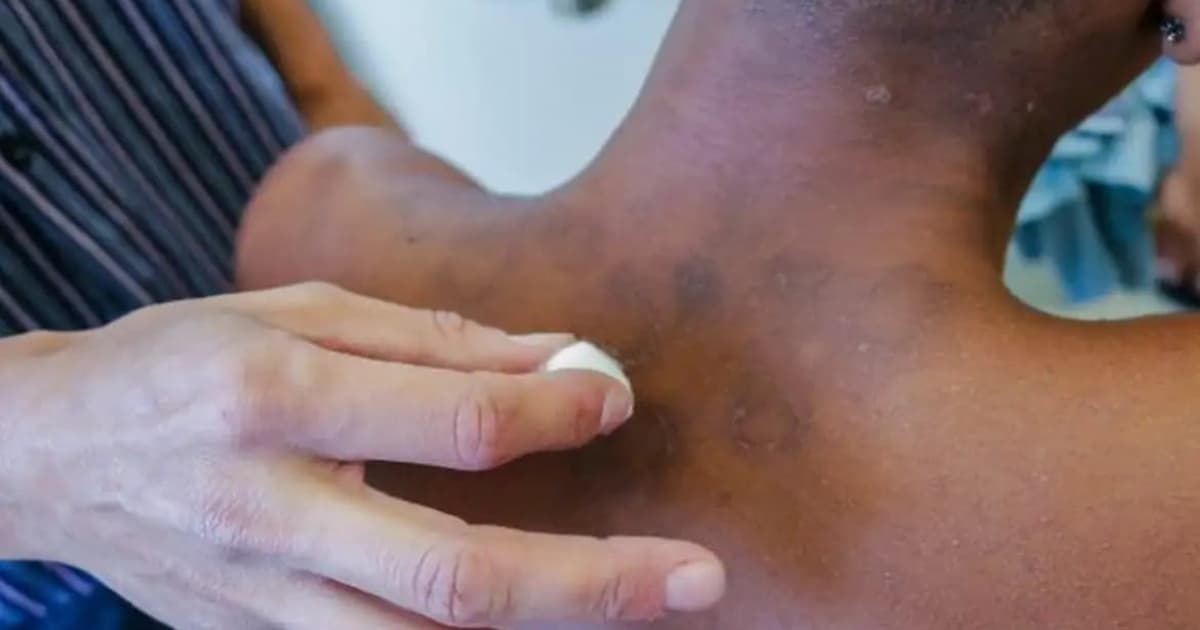
Foto: SMS de Mesquita/RJ
A Agência Nacional de Vigilância Sanitária (Anvisa) publicou,
nesta segunda-feira (14), a autorização para o início de testes que têm o
intuito de analisar a segurança, a tolerabilidade e a imunogenicidade da vacina
LepVax contra a hanseníase.
Segundo a Anvisa, na fase 1b do ensaio clínico, serão
incluídos 30 participantes recrutados no Ambulatório Souza Araújo, no Rio de
Janeiro. O imunizante será aplicado após a administração intramuscular de
2 μg ou 10 μg da vacina nos dias 0, 28 e 56.
Após os resultados registrados nessa fase, a Fiocruz poderá
submeter o pedido de autorização para a realização da fase 2a, que contemplará
pacientes com hanseníase paucibacilar (PB). A fase pré-clínica e a fase 1a
do desenvolvimento clínico foram testadas nos Estados Unidos e a vacina foi
classificada como segura em adultos saudáveis quando administrada por via
intramuscular em todas as doses testadas.
A hanseníase, conhecida antigamente como lepra, é causada por
infecção com a bactéria Mycobacterium leprae. A doença pode atingir
principalmente os olhos, a pele, o nariz e os nervos periféricos. Entre os
sintomas estão manchas claras ou vermelhas na pele com diminuição da
sensibilidade, dormência e fraqueza nas mãos e nos pés. A enfermidade pode ser
curada com 6 a 12 meses de terapia com vários medicamentos. No entanto, ainda
não existe um imunizante para combater a doença.

